Agricultura
Viaje intra y extracelular del ácido salicílico de fitohormonas

El ácido salicílico (SA) es una hormona vegetal que se ha descrito que desempeña un papel esencial en la activación y regulación de múltiples respuestas al estrés biótico y abiótico. En particular, durante las interacciones planta-microbio, como parte de los mecanismos de defensa, SA se acumula inicialmente en el tejido infectado local y luego se extiende por toda la planta para inducir resistencia sistémica adquirida en las partes distales no infectadas de la planta.
SA puede producirse por las vías biosintéticas de fenilalanina o isocorismato. El primero ocurre en el citosol, mientras que el segundo ocurre en los cloroplastos. Una vez sintetizados, los niveles de SA libre están regulados por una serie de modificaciones químicas que producen formas inactivas, incluida la glicosilación, metilación e hidroxilación a ácidos dihidroxibenzoicos.
La SA glicosilada se almacena en la vacuola, hasta que sea necesario para activar las respuestas activadas por SA. Toda esta información sugiere que los niveles de SA están bajo un estricto control, incluyendo su movimiento intra y extracelular que debe ser coordinado por la acción de los transportadores. Sin embargo, nuestro conocimiento sobre este tema es aún muy limitado. En esta revisión, describimos los esfuerzos más significativos realizados hasta la fecha para identificar los mecanismos moleculares involucrados en el transporte de SA en toda la planta.
Además, proponemos nuevas alternativas que podrían ayudar a comprender el viaje de esta importante fitohormona en el futuro. En esta revisión, describimos los esfuerzos más significativos realizados hasta la fecha para identificar los mecanismos moleculares involucrados en el transporte de SA en toda la planta. Además, proponemos nuevas alternativas que podrían ayudar a comprender el viaje de esta importante fitohormona en el futuro. En esta revisión, describimos los esfuerzos más significativos realizados hasta la fecha para identificar los mecanismos moleculares involucrados en el transporte de SA en toda la planta. Además, proponemos nuevas alternativas que podrían ayudar a comprender el viaje de esta importante fitohormona en el futuro.
Descubrimiento del ácido salicílico
El ácido salicílico (SA) pertenece a un grupo de moléculas denominadas colectivamente salicilatos, que son compuestos fenólicos sintetizados por plantas, que poseen un anillo aromático y un grupo hidroxilo. Incluso antes de que los salicilatos fueran identificados químicamente, durante miles de años, los humanos los usaron como analgésicos ( Klessig et al., 2018 ). La primera evidencia conocida de este uso se descubrió en la placa dental de fósiles de neandertales de la cueva de El Sidrón ( Weyrich et al., 2017 ). Estos fósiles contenían restos de corteza de álamo, lo que sugiere que los individuos masticaron la planta para aliviar el dolor de los abscesos dentales. El uso de plantas que contienen salicilatos como analgésicos se puede encontrar en muchas culturas antiguas de Europa, Asia y América ( Vlot et al., 2009). Sin embargo, no fue hasta 1828 que Johann A. Buchner purificó la salicina de la corteza de sauce. Posteriormente, alrededor de 1838, la salicina se separó en un azúcar y un compuesto aromático que podría convertirse en un ácido, llamado ácido salicílico (ácido 2-hidroxibenzoico), en honor al nombre latino del sauce blanco Salix alba por Raffaele Piria ( Vlot et al. ., 2009 ; Kumar, 2014 ). Free SA es poco soluble en agua y muy soluble en disolventes orgánicos polares, con un valor de pH de una solución acuosa saturada de 2,4. SA emite fluorescencia a 412 nm cuando se excita a 301 nm y esta propiedad se ha utilizado para detectarlo en varias plantas ( Raskin, 1992 ).
En 1859, Hermann Kolbe y sus compañeros de trabajo sintetizaron SA, lo que provocó un aumento en su consumo debido a la fácil disponibilidad y la disminución de costos. Luego, años después, con el fin de evitar los efectos secundarios inducidos por el consumo de SA (irritación y sangrado en el estómago), Felix Hoffmann informó que el ácido acetilsalicílico, causó menos daño al sistema digestivo, lo que finalmente desembocó en el producto que hoy en día se usa en todo el mundo. – aspirina ( Vlot et al., 2009 ; Klessig et al., 2018 ). Aunque los efectos y beneficios de la aspirina en humanos para tratar la fiebre, el dolor o la hinchazón y para reducir el riesgo de ataque cardíaco, accidente cerebrovascular y ciertos cánceres, se han descrito y estudiado bien ( Klessig et al., 2018)), su papel como metabolito secundario en la biología vegetal no se caracterizó hasta finales del siglo XX.
La hormona vegetal SA
Se ha descrito que las hormonas vegetales desempeñan funciones biológicas esenciales en la regulación del crecimiento, el desarrollo, la reproducción y la supervivencia de las plantas; y muchos de estos mecanismos están regulados por vías de comunicación cruzada y transducción de señales, dentro de las cuales las hormonas vegetales cumplen funciones centrales ( Verhage et al., 2010 ; De Vleesschauwer et al., 2013 ).
Durante muchos años, SA fue considerado solo uno de los miles de compuestos fenólicos producidos por las plantas, otro metabolito secundario con una función biológica relativamente poco importante ( Raskin, 1992 ; Métraux y Raskin, 1993 ). Sin embargo, en 1974, SA se describió por primera vez como una molécula de señalización móvil localizada en el floema, que puede inducir la floración de Xanthium strumarium y Lemna gibba , lo que sugiere un papel como hormona vegetal ( Cleland, 1974 ; Cleland y Ajami, 1974 ). Sin embargo, la evidencia de que SA era una fitohormona provino de la descripción de su papel durante la termogénesis en el lirio vudú ( Sauromatum guttatum ) (Raskin y col., 1989 ). Los autores identificaron un aumento de 100 veces de SA endógeno durante este evento que también puede ser estimulado específicamente por SA exógeno o sus derivados, pero no por otros compuestos estructuralmente relacionados. Después de esta caracterización inicial, múltiples informes estudiaron el papel de SA como fitohormona, incluida su participación en la resistencia y tolerancia a muchos estreses abióticos, incluido el ozono, la radiación UV, el paraquat, el calor, el frío, el metal y los estreses salinos / osmóticos ( Horváth et al., 2007 ; Yuan y Lin, 2008 ; Rivas-San Vicente y Plasencia, 2011 ; Dempsey y Klessig, 2017). Además, existe evidencia de que la aplicación de SA afecta múltiples aspectos del crecimiento y desarrollo de las plantas, incluyendo la germinación de semillas, crecimiento vegetativo, floración, rendimiento de frutos, senescencia, cierre de estomas, termogénesis, fotosíntesis, respiración, cambios en la vía respiratoria alternativa, glucólisis. y el ciclo de Krebs ( Khan et al., 2015 ; Dempsey y Klessig, 2017 ; Klessig et al., 2018 ). Sin embargo, una de las respuestas inducidas por SA mejor caracterizadas es la que involucra interacciones planta-microbio, que se describe a continuación.
SA, un regulador esencial de las interacciones planta-microbio
Las plantas interactúan constantemente con millones de microorganismos, incluidas bacterias, levaduras, hongos y virus ( Lindow y Brandl, 2003 ; Baldwin et al., 2017 ). En respuesta, se establece un diálogo íntimo entre plantas y microbios, que modifica el crecimiento y desarrollo de los patógenos y la inducción de las respuestas de defensa de las plantas ( Aragón et al., 2017). La primera línea de defensa se agrupa en la inmunidad innata, que se puede dividir en inmunidad activada por patrones moleculares asociada a patógenos (PTI) e inmunidad activada por efectores (ETI). Durante la PTI, se inducen la acumulación de especies reactivas de oxígeno (ROS), las cascadas de señalización dependientes de la proteína quinasa activada por mitógenos (MAPK) y la reprogramación transcripcional, mientras que durante la ETI, la inducción de las respuestas de PTI anteriores es más fuerte y / o más rápida, que generalmente es acompañada de muerte celular programada o respuesta hipersensible en el sitio de infección ( Boller y Felix, 2009 ; Zipfel, 2014 ; Conrath et al., 2015 ). El efecto de ETI y PTI puede bloquear la infección de patógenos no adaptados, tanto en el tejido infectado localmente como sistémicamente en hojas no infectadas (Craig et al., 2009 ). Después de estos eventos tempranos, se desencadenan respuestas de defensa secundarias o tardías, incluida la activación de vías de señalización inducidas por hormonas. Las principales hormonas involucradas durante la inmunidad innata son SA, ácido jasmónico y etileno ( Yang et al., 2013 ). Sin embargo, el ácido abscísico, las giberelinas, las auxinas, las citoquininas y los brasinoesteroides también pueden funcionar como moduladores de las redes de señalización inmunológica de las plantas ( Pieterse et al., 2009 , 2012 ).
El papel de SA durante las interacciones planta-microbio, se registró por primera vez en plantas de tabaco y pepino en 1990. Las plantas con una mayor resistencia al virus del mosaico del tabaco (TMV) mostraron una fuerte acumulación de SA, mientras que con las plantas susceptibles a TMV, Los niveles de SA se redujeron significativamente ( Malamy et al., 1990 ). Se han publicado múltiples informes que muestran el efecto de SA regulando las interacciones entre plantas y microbios y revisiones recientes han hecho una descripción detallada de esta regulación ( Dempsey y Klessig, 2017 ; Klessig et al., 2018 ). A continuación, describimos algunos de los hallazgos más relevantes.
Después de la observación inicial con plantas de tabaco y pepino, varios estudios encontraron que las plantas de tabaco y Arabidopsis thaliana transformadas con el gen bacteriano nahG , que codifica una salicilato hidroxilasa bacteriana que degrada SA a catecol, mostraron mayor susceptibilidad a patógenos ( Gaffney et al., 1993 ; Delaney y col., 1994 ; Lawton y col., 1995 ). Mediante análisis genéticos y bioquímicos, la vía de señalización dependiente de SA se ha caracterizado durante los últimos años ( Figura 1 ). Recientemente, la proteína NPR1 fue descrita como el receptor de SA ( Wu et al., 2012). Plantas no infectadas, con bajos niveles de SA, NPR1 forma un complejo oligomérico localizado en el citosol ( Figura 1A ), modulando la diafonía entre SA y ácido jasmónico, pero no induciendo genes de defensa dependientes de SA ( Spoel et al., 2003 ). Sin embargo, tras la infección por patógenos o el tratamiento con SA exógeno, se produce un cambio en el sistema redox celular, que se ha asociado con la supresión de las respuestas JA desencadenada por SA ( Holuigue et al., 2016 ), que induce la disociación del complejo NPR1 en monómeros. , por la reducción de enlaces disulfuro ( Figura 1B ) ( Tada et al., 2008). Estas formas monoméricas pueden luego translocarse al núcleo, donde interactúan con factores de transcripción de tipo TGA de cremallera de leucina básica (bZIP), induciendo la modificación del transcriptoma, incluida la activación transcripcional de los genes relacionados con la defensa, como PR-1 ( Figura 1B ) ( Fu y Dong, 2013 ; Birkenbihl et al., 2017 ).
 Figura 1. Regulación de la expresión génica mediada por SA para la defensa de las plantas. (A) SA (esferas de plata) se sintetiza por las vías de la fenilalanina amoniaco liasa (PAL) o del isocorismato (IC). A niveles bajos de SA, NPR1 se presenta en el citosol como un oligómero unido por puentes disulfuro. (B) A alta concentración intracelular de SA, el aumento de SA modifica el potencial de reducción celular, lo que conduce a cambios en la estructura de NPR1 a monómeros a través de la reducción de los puentes intermoleculares por un cambio en redox. Esto permite que NPR1 entre en el núcleo, donde se une a factores de transcripción de TGA específicos que inducen la expresión de genes de respuesta defensiva inducidos por SA.
Figura 1. Regulación de la expresión génica mediada por SA para la defensa de las plantas. (A) SA (esferas de plata) se sintetiza por las vías de la fenilalanina amoniaco liasa (PAL) o del isocorismato (IC). A niveles bajos de SA, NPR1 se presenta en el citosol como un oligómero unido por puentes disulfuro. (B) A alta concentración intracelular de SA, el aumento de SA modifica el potencial de reducción celular, lo que conduce a cambios en la estructura de NPR1 a monómeros a través de la reducción de los puentes intermoleculares por un cambio en redox. Esto permite que NPR1 entre en el núcleo, donde se une a factores de transcripción de TGA específicos que inducen la expresión de genes de respuesta defensiva inducidos por SA.
Además, la actividad de NPR1 está regulada por la degradación mediada por proteasomas. Este proceso lo llevan a cabo los parálogos NPR1, NPR3 y NPR4, que son adaptadores para la ligasa de ubiquitina E3 Cullin 3 y median la degradación de NPR1 de una manera dependiente de SA. En células no infectadas, cuando los niveles de SA son bajos, se propone que NPR4 mantenga niveles bajos de NPR1. Sin embargo, después de la infección, cuando aumentan los niveles de SA, se interrumpe la interacción NPR4-NPR1, lo que permite la acumulación de NPR1. Además, cuando el nivel de SA es extremadamente alto, NPR3 se une a NPR1 y conduce a la degradación de NPR1 ( Spoel et al., 2009 ; Fu et al., 2012 ; Dempsey y Klessig, 2017). El recambio de NPR1 asegura una activación de defensa correcta y es necesario para la inducción completa de genes diana y el establecimiento de respuestas inducidas por SA ( Spoel et al., 2009 ). Sin embargo, hasta ahora solo la función del adaptador de ubiquitina ligasa se ha atribuido a NPR3 y NPR4, pero también podrían estar involucradas en la regulación transcripcional de genes de defensa inducidos por SA. Las plantas de Arabidopsis thaliana que albergan versiones mutantes de NPR3 y NPR4, incapaces de unirse a SA, mostraron una represión constitutiva de las respuestas inmunitarias inducidas por SA y una mayor expresión de genes de defensa inducida por SA, respectivamente ( Ding, 2018 ).
Después de estas respuestas iniciales desencadenadas por SA en el tejido local infectado / tratado, las plantas pueden inducir un síndrome de defensa duradero y de amplio espectro llamado resistencia sistémica adquirida (SAR), que incluye la acumulación de proteínas PR y la inducción de una biosíntesis adicional de SA ( Mishina y Zeier, 2007 ). El SAR promueve un cebado de los mecanismos de defensa que es una respuesta más rápida y fuerte a una infección secundaria infligida por virus, patógenos bacterianos y fúngicos ( Vlot et al., 2009 ; Conrath et al., 2015 ). El derivado químico de SA (MeSA) se describió inicialmente como la señal móvil responsable de inducir SAR ( Rasmussen et al., 1991 ; Park et al., 2007 ; Vlot et al., 2009). Sin embargo, aunque varios informes sugieren que SA es una molécula importante para inducir SAR, no es la única ( Smith et al., 1991 ; Vernooij et al., 1994 ). Trabajos posteriores han descrito que junto con SA, otros compuestos participan como inductores de SAR incluyendo: ácido dicarboxílico ácido azelaico (AzA), glicerol-3-fosfato (G3P), deshidroabietinal (DA) y ácido pipecólico (Pip) [revisado por Singh et al. (2017) ]. Sin embargo, estos resultados muestran el importante papel de SA durante las interacciones entre plantas y patógenos.
La biosíntesis y el almacenamiento de SA están compartimentados
El ácido salicílico probablemente esté presente en todas las plantas, sin embargo, su concentración puede fluctuar ampliamente entre las especies e incluso entre miembros de la misma familia ( Raskin et al., 1990 ). Por ejemplo, las hojas de tabaco pueden contener <100 ng / g de peso fresco (FW) de SA, mientras que en la papa pueden llegar a 10 μg / g FW ( Malamy et al., 1992 ; Coquoz et al., 1998 ). En la planta modelo Arabidopsis thaliana , el nivel basal de SA se ha cuantificado entre 0,250 y 1 μg / g FW ( Nawrath y Métraux, 1999 ; Wildermuth et al., 2001 ). Varias revisiones han realizado recientemente una descripción detallada de la biosíntesis de SA ( Dempsey et al., 2011 ; Dempsey y Klessig, 2017 ;Klessig et al., 2018 ). Hasta la fecha, la biosíntesis de SA no se ha definido completamente, sin embargo, la evidencia genética y bioquímica señaló que SA se puede producir a partir de dos vías independientes y compartimentadas: la vía del isocorismato (IC) localizada en los plástidos y la fenilalanina amoniaco liasa ( PAL) que tiene lugar en el citosol ( Figura 2 ). Ambas vías comienzan por la acumulación de ácido corísmico, producido por la biosíntesis del ácido shikímico. En la vía de la CI, el ácido corísmico se convierte en ácido isocorísmico (CI) por la isocorismato sintasa y luego, a través de la actividad de la isocorismato piruvato liasa (IPL) SA se produce en el cloroplasto y luego se exporta al citosol ( Fragnière et al., 2011).). Por otro lado, en la vía PAL, el ácido prefénico se produce a partir del ácido corísmico por la corismato mutasa (CM), luego se reduce a L -fenilalanina (Phe) que se convierte en ácido trans- cinámico ( t -CA) por la actividad PAL. . A partir de t -CA se pueden producir dos metabolitos: ácido orto- curmárico ( o -CA) y benzaldehído. SA se puede sintetizar directamente a partir de o -CA, mientras que el benzaldehído se transforma primero en ácido benzoico (BA) por la aldehído oxidasa (AAO) y luego en SA por la actividad del ácido benzoico 2-hidroxilasa (BA2H) ( Figura 2). Una vez que se sintetiza SA, sus niveles son regulados por una serie de modificaciones químicas, para producir formas inactivas, incluyendo éster de saliciloil glucosa (SGE), SA O-β-glucósido (SAG), salicilato de metilo (MeSA) y salicilato de metilo O- β-glucósido (MeSAG). Estas moléculas inactivas se pueden almacenar hasta que se requieran para activar las respuestas desencadenadas por SA.
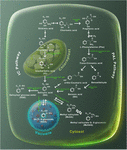 Figura 2. Metabolismo de SA. Las plantas utilizan dos vías para producir SA, la fenilalanina amoniaco liasa (PAL) y el isocorismato (IC). El ácido shikímico sirve como precursor en ambas vías. La ruta PAL se realiza en el citosol, donde el ácido shikímico se transforma en ácido corísmico y luego en fenilalanina por acción de la enzima mutasa corísmica. Más tarde, la enzima PAL usa fenilalanina para producir ácido trans- cinámico que a su vez se convierte en orto-ácido cumarico y benzaldehído. Posteriormente, el benzaldehído se convierte en ácido benzoico (BA) por la enzima aldehído oxidasa (AAO). BA se transforma en SA mediante una reacción catalizada por la enzima hidroxilasa del ácido benzoico (BA2H). La ruta IC tiene lugar en el cloroplasto: la isocorismato sintasa sintetiza SA para generar isocorismato, que luego se transforma en SA mediante la acción de las enzimas isocorismato piruvato liasa. Los glucósidos de ácido salicílico (SAG y SGE) son producidos por glucosiltransferasas (SAGT); mientras que la metilación de SA es realizada por la enzima metiltransferasas. Se muestran las estructuras químicas y su localización subcelular de sustratos y derivados SA.
Figura 2. Metabolismo de SA. Las plantas utilizan dos vías para producir SA, la fenilalanina amoniaco liasa (PAL) y el isocorismato (IC). El ácido shikímico sirve como precursor en ambas vías. La ruta PAL se realiza en el citosol, donde el ácido shikímico se transforma en ácido corísmico y luego en fenilalanina por acción de la enzima mutasa corísmica. Más tarde, la enzima PAL usa fenilalanina para producir ácido trans- cinámico que a su vez se convierte en orto-ácido cumarico y benzaldehído. Posteriormente, el benzaldehído se convierte en ácido benzoico (BA) por la enzima aldehído oxidasa (AAO). BA se transforma en SA mediante una reacción catalizada por la enzima hidroxilasa del ácido benzoico (BA2H). La ruta IC tiene lugar en el cloroplasto: la isocorismato sintasa sintetiza SA para generar isocorismato, que luego se transforma en SA mediante la acción de las enzimas isocorismato piruvato liasa. Los glucósidos de ácido salicílico (SAG y SGE) son producidos por glucosiltransferasas (SAGT); mientras que la metilación de SA es realizada por la enzima metiltransferasas. Se muestran las estructuras químicas y su localización subcelular de sustratos y derivados SA.
En Arabidopsis thaliana , la glucosilación de SA se realiza mediante la acción de las enzimas UDP-glucosiltransferasa UGT74F1 y UGT74F2 ( Lim et al., 2002 ; Dean y Delaney, 2008 ). Ambos genes UGT74F1 y UGT74F2 son inducidos por SA y localizados en el citosol ( Dean y Delaney, 2008 ; Park et al., 2017 ). El mutante ugt74f1 acumula menos SAG que el mutante ugt74f2 y las plantas de tipo salvaje, mientras que SGE no se formó en el fondo ugt74f2 ( Dean y Delaney, 2008). Se ha demostrado que UGT74F1 cataliza la formación de SAG y formas UGT74F2 principalmente SGE, pero también sintetiza SAG ( Dean y Delaney, 2008 ; Dempsey et al., 2011 ). Por otro lado, SA produce MeSA por la acción de una carboxil metiltransferasa (SAMT) ( Ross et al., 1999 ; Zubieta et al., 2003 ). En Arabidopsis thaliana , AtBSMT1 codifica una carboxil metiltransferasa, que puede usar BA o SA como sustratos para formar MeSA ( Chen et al., 2003 ) ( Figura 2 ). Se observó que la expresión del gen AtBSMT1 y, por lo tanto, la producción de MeSA se indujeron en Arabidopsis thalianahojas por tratamiento con alameticina, un péptido formador de poros que emula el daño de patógenos ( Chen et al., 2003 ). Por lo tanto, se sugiere que AtBSMT1 realice la producción de MeSA principalmente durante la infección por patógenos ( Liu et al., 2009 ). Los mutantes alterados en la expresión de AtBSMT1 no acumularon MeSA después del ataque de patógenos, mientras que la sobreexpresión de AtBSMT1 condujo a una acumulación incrementada de MeSA en la zona de infección ( Liu et al., 2009 ). Curiosamente, la sobreexpresión y los mutantes de AtBSMT1 no pudieron acumular SA o SAG en las hojas distales y no establecieron SAR ( Liu et al., 2009 ). Probablemente, la sobreexpresión de AtBSMT1conduce a una conversión excesiva de SA libre en MeSA, lo que evita la acumulación necesaria de SA para desarrollar SAR en las hojas sistémicas. Se hizo una observación similar cuando las plantas de Arabidopsis thaliana sobreexpresan el gen OsBSMT1 del arroz, que acumuló MeSA de forma constitutiva y no acumuló SA o SAG y fueron vulnerables a enfermedades patógenas ( Koo et al., 2007 ). Sorprendentemente, el aumento en los niveles de MeSA liberados por plantas transgénicas fue suficiente para provocar SAR en plantas de tipo silvestre cercanas en un proceso independiente de ICS1 ( Koo et al., 2007 ). Finalmente, en plantas infectadas con el virus Nicotiana benthamiana , la SAR se vio afectada cuando se silenció el gen SAMT ( Zhu et al., 2014).
Tomados en conjunto, el hecho de que SA se produce en el cloroplasto y en el citosol, su forma inactiva (SAG) se almacena en diferentes compartimentos celulares ( Figura 2 ) y luego se extiende por toda la planta para participar en SAR, sugiere un intra y extracelular. movimiento, que debe ser coordinado por la acción de los transportistas.
El viaje de SA
De manera similar, las hormonas animales, las fitohormonas se sintetizan con frecuencia en un lugar diferente al que desarrollan su función, por lo que requieren una comunicación local o de larga distancia. Las plantas emplean numerosos mecanismos de entrega que dependen de la distancia y dirección del transporte ( Bonnemain et al., 2013 ; Park et al., 2017 ). En las siguientes secciones, examinamos los avances más interesantes sobre el transporte intracelular, de célula a célula y de larga distancia de SA ( Tabla 1 y Figura 3 ).
 Figura 3. Un modelo dinámico propuesto de SA libre y conjugado. (Hoja inferior) La SA sintetizada por las vías ICS y PAL se muestra en esferas grises. En el cloroplasto, SA se transloca al citosol a través de transportadores EDS5 (portador rojo). Una vez extruido, SA se conjuga con glucosa para formar SAG o SGE (esferas rojas y amarillas, respectivamente). Posteriormente, SAG es transportado a la vacuola por sistemas transportadores ABC / anti-transportadores H + (transportadores amarillos). SA puede extenderse al apoplasto mediante un sistema mediado por portadores (portadores verdes). SA se convierte en MeSA volátil (esferas de color púrpura) por la enzima carboxil metiltransferasa (SAMT). (Madre)El transporte de floema SA puede basarse en un transporte celular externo simplástico, la ingesta de apoplasto del floema a través de un mecanismo de trampa de iones y una ingesta de apoplasto mediada por un sistema portador. MeSA también se puede encontrar en el floema. (Hoja superior) Después de un ataque de patógenos, los niveles de SA aumentan en el tejido infectado primario. SA se convierte en MeSA (esferas púrpuras). El MeSA acumulado se transloca al tejido sistémico no inoculado. MeSA se desmetila para formar SA e induce la síntesis de novo de SA en el tejido distal.
Figura 3. Un modelo dinámico propuesto de SA libre y conjugado. (Hoja inferior) La SA sintetizada por las vías ICS y PAL se muestra en esferas grises. En el cloroplasto, SA se transloca al citosol a través de transportadores EDS5 (portador rojo). Una vez extruido, SA se conjuga con glucosa para formar SAG o SGE (esferas rojas y amarillas, respectivamente). Posteriormente, SAG es transportado a la vacuola por sistemas transportadores ABC / anti-transportadores H + (transportadores amarillos). SA puede extenderse al apoplasto mediante un sistema mediado por portadores (portadores verdes). SA se convierte en MeSA volátil (esferas de color púrpura) por la enzima carboxil metiltransferasa (SAMT). (Madre)El transporte de floema SA puede basarse en un transporte celular externo simplástico, la ingesta de apoplasto del floema a través de un mecanismo de trampa de iones y una ingesta de apoplasto mediada por un sistema portador. MeSA también se puede encontrar en el floema. (Hoja superior) Después de un ataque de patógenos, los niveles de SA aumentan en el tejido infectado primario. SA se convierte en MeSA (esferas púrpuras). El MeSA acumulado se transloca al tejido sistémico no inoculado. MeSA se desmetila para formar SA e induce la síntesis de novo de SA en el tejido distal.
Transporte intracelular: de la síntesis de SA al almacenamiento
La síntesis de SA, inducida por estrés biótico y abiótico, se localiza en el cloroplasto y luego se transporta al citosol ( Dean et al., 2005 ; Garcion et al., 2008 ; Fragnière et al., 2011 ). Sin embargo, el mecanismo molecular involucrado en este transporte activo fue durante mucho tiempo desconocido. A principios de 2000, dos de Arabidopsis thaliana mutantes, llamado S A i nduction- d eficient ( SID1 y SID2 ) fueron identificados ( Nawrath y Métraux, 1999 ). SidSe describió que los mutantes estaban alterados en la biosíntesis de SA y mostraban una mayor susceptibilidad a la enfermedad frente a patógenos bacterianos y fúngicos ( Nawrath y Métraux, 1999 ). Se identificó que sid1 era alélico a la SUSCEPTIBILIDAD 5 MEJORADA A LAS ENFERMEDADES ( EDS5 ), un miembro de la familia de transportadores de extrusión de toxinas y múltiples fármacos (MATE) ( Nawrath y Métraux, 1999 ; Nawrath et al., 2002 ). Las plantas de Arabidopsis thaliana que sobreexpresan EDS5 muestran una mayor resistencia a los virus, validando el papel de EDS5 durante las respuestas de defensa de las plantas ( Ishihara et al., 2008). Además, otros informes han demostrado que EDS5 está localizado en la membrana de la envoltura del cloroplasto, lo que sugiere que podría estar involucrado en el transporte de SA ( Serrano et al., 2013 ; Yamasaki et al., 2013 ). Al analizar el movimiento de SA radiomarcado en cloroplastos aislados que sobreexpresan EDS5 de Arabidopsis thaliana , y en un sistema heterólogo de levadura, se confirmó que EDS5 participa en la exportación de SA del cloroplasto al citosol ( Serrano et al., 2013 ).
Curiosamente, el homólogo de EDS5 ( EDS5H ) también muestra una ubicación de envoltura cloroplástica, pero, sin embargo, no es inducido ni por patógenos ni por la aplicación de SA exógeno y su eds5h mutante no se altera en la biosíntesis de SA ( Parinthawong et al., 2015 ) . Es muy probable que EDS5H transporte otros compuestos fenólicos, pero no SA, lo que sugiere que el sistema de transporte de SA mediado por proteínas solo lo realizan portadores específicos ( Parinthawong et al., 2015 ). Esta evidencia sugiere que EDS5, hasta donde sabemos, es el transportador de plantas SA único identificado hasta ahora involucrado en su movimiento del cloroplasto al citosol.
Una vez sintetizado o transportado en el citosol, el SA puede someterse a conjugación con glucosa para convertirlo en una forma inactiva que sea soluble en agua para su almacenamiento ( Figura 3 ). Dependiendo de dónde se adhiera la glucosa, ya sea el grupo hidroxilo o el grupo carboxilo, SA se puede transformar en SA-glucósido (SAG) o éster de glucosa SA (SGE), respectivamente ( Lim et al., 2002 ; Dean et al., 2003 , 2005 ; Dean y Mills, 2004 ; Park et al., 2007 ). Se sabe que los glucósidos, como los glucósidos flavonoides y SAG, son formas estables para el almacenamiento de otros compuestos fenólicos pequeños, mientras que los ésteres de glucosa, como SGE, pueden actuar como sustratos intermedios en una vía biosintética (Petrussa et al., 2013 ; Vaca et al., 2017 ). Curiosamente, los informes en tabaco y álamo sugieren que el éster de glucosa de BA y SGE podrían ser precursores de la formación de SA, lo que indica que SGE podría acumularse en el citosol para usarse como un precursor listo para usar de SA mientras que SAG se acumula en vacuola hasta que la planta la necesite ( Chong et al., 2001 ; Ruuhola y Julkunen-Tiitto, 2003 ).
Se ha demostrado que SAG se transporta a la vacuola en varias especies de plantas, como la soja, el tabaco, la remolacha roja y Arabidopsis thaliana ( Tabla 1 ) ( Dean y Mills, 2004 ; Dean et al., 2005 ; Vaca et al., 2017 ). Para la soja, SAG parece ser exportado a la vacuola por transportadores de casete de unión a ATP (ABC) ( Dean y Mills, 2004 ). En el tabaco y la remolacha roja, el transporte se realiza mediante antiportadores H + ( Dean et al., 2005 ). Mientras que en Arabidopsis thaliana , SAG se almacena en la vacuola y SGE solo se encuentra en el citoplasma ( Vaca et al., 2017). Un análisis de captación de SAG radiomarcado, en vacuolas de Arabidopsis thaliana , reveló que se transloca hacia la vacuola a través de un proceso dependiente de MgATP ( Vaca et al., 2017 ). Además, el transporte vacuolar de SAG fue bloqueado por inhibidores de transportadores ABC y sistemas antiportadores H + , lo que indica que el transporte de SA glicosilado puede ser realizado por este tipo de bombas ( Vaca et al., 2017 ).
El SA-glucósido se reconvierte en la forma activa de SA cuando se hidroliza. En el tabaco, SAG se reconvierte en SA en el apoplasto ( Hennig et al., 1993 ), lo que tiene sentido con la localización extracelular de β-glucosidasas en plantas dicotiledóneas y también corresponde al papel que desempeñan estas enzimas durante las interacciones entre patógenos vegetales ( Morant et al., 2008 ). Sin embargo, todavía se desconoce si el SAG vacuolar se transporta al apoplasto y / o si se libera después de una respuesta inducida por patógenos. Además, no se puede descartar que las enzimas intracelulares puedan hidrolizar SAG en condiciones especiales ( Dempsey et al., 2011 ). En conjunto, estas observaciones indican que el nivel intracelular de SA y sus formas inactivas están bajo el control de los transportadores.
Transporte de célula a célula: entrada y salida de SA
Una vez que SA se sintetiza dentro de las células, el siguiente paso en el viaje de SA es su diseminación a las células vecinas ( Figura 3 ) ( Kawano et al., 2004 ). A menudo, SA se propaga a través del apoplasto ( Lim et al., 2016 ; Singh et al., 2017 ). Debido a sus características químicas, tales como ácido débil y escasa solubilidad en agua, SA atraviesa las membranas plasmáticas de células animales y vegetales por difusión dependiente del pH y mecanismos mediados por portadores ( Chatton y Roch-Ramel, 1992 ; Takanaga et al., 1994 ; Chen et al., 2001 ; Emoto et al., 2002 ; Bonnemain et al., 2013). En los mamíferos, un transportador de monocarboxilato se localiza en la membrana plasmática celular ( Enerson y Drewes, 2003 ). En plantas, se ha reportado la afluencia de SA radiomarcado en la planta acuática Lemna gibba , donde alrededor del 90% de 10 μM SA aplicado al medio fue absorbido en media hora, sin embargo, se desconocen los mecanismos por los cuales se internalizó el SA ( Ben-Tal y Cleland, 1982 ). Sin embargo, después de la absorción, SA se localizó en el citosol o en la vacuola y no se observó ningún otro transporte de plasmodesmos en las células de L. gibba ( Ben-Tal y Cleland, 1982 ). Es probable que SA se conjugó rápidamente con glucosa y se almacenó en vacuolas.
Curiosamente, la absorción de SA fue más rápida en una suspensión de células de tabaco que en las plantas de L. gibba , tomando hasta 200 μM de SA en solo 5 minutos ( Chen et al., 2001 ). Sin embargo, después de 5 h, más del 90% del SA radiomarcado absorbido se liberó al medio. La entrada de SA podría inhibirse añadiendo un agente quelante (EGTA), pero la salida se restauró mediante la adición de Ca 2+ y, además, un inhibidor de la síntesis de proteínas bloqueó la excreción de SA ( Chen et al., 2001 ; Kawano et al., 2004 ). Los autores sugieren la presencia de un transportador de salida de SA que puede inducirse a concentraciones elevadas de SA y que puede involucrar a ROS, Ca 2+ , de-novosíntesis de proteínas y una vía de señalización de fosforilación de proteínas ( Chen et al., 2001 ; Kawano et al., 2004 ; Bonnemain et al., 2013 ). Sin embargo, también se ha propuesto un portador de salida de SA constitutivo involucrado durante concentraciones bajas de SA, independiente de ROS, Ca2 + y la señalización en cascada de proteína quinasa ( Kawano et al., 2004 ; Bonnemain et al., 2013 ).
Transporte de larga distancia
Junto con el ácido azelaico (AzA), glicerol-3-fosfato (G3P), metil jasmonato (MeJA) y ácido pipecólico (Pip), SA participa como un inductor crítico de larga distancia para SAR ( Conrath et al., 2015 ; Klessig et al., 2018 ). Se observó una rápida translocación de SA radiomarcada, inyectada al final de los pecíolos de las hojas de tabaco, en las hojas superiores e inferiores vecinas sistémicas ( Ohashi et al., 2004 ). Cuando 14 BA C-marcado se aplica a los cotiledones de pepino infectadas con el virus de la necrosis del tabaco, etiquetado SA fue encontrado posteriormente en el floema y en la hoja infectada superior ( Mölders et al., 1996 ). Durante la infección por patógenos, SA se acumula en el floema, a través del apoplasto en Arabidopsis thaliana.y plantas de tabaco ( Yalpani et al., 1991 ; Zhu et al., 2014 ; Lim et al., 2016 ). Además, se ha informado de que la translocación de SA radiomarcada se produce desde hojas inoculadas con virus del tabaco hacia zonas distales no infectadas ( Shulaev et al., 1995 ). La translocación de SA por el xilema también se ha informado en plántulas de tabaco y Ricinus communis , aunque la contribución del xilema en el transporte mediado por SA para desarrollar SAR aún no está clara ( Ohashi et al., 2004 ; Rocher et al., 2006 ).
En las plántulas de Ricinus communis , los mecanismos de transporte del floema SA comprenden un sistema de transporte dependiente del pH de alta especificidad, que puede colocarse en los tejidos internos, principalmente en las venas de los cotiledones ( Tabla 1 ) ( Rocher et al., 2006 , 2009 ). Los autores sugieren que la carga de floema SA puede basarse en un transporte celular externo simplástico, ingesta de apoplasto del floema, a través de un mecanismo de trampa de iones y una ingesta de apoplasto mediada por un sistema portador ( Figura 3 ) ( Rocher et al., 2009 ).
La principal barrera para prevenir la libre difusión de SA es la cutícula de la planta ( Niederl et al., 1998 ; Ohashi et al., 2004 ). De manera controvertida, es bien sabido que la aplicación exógena de SA, ya sea por cebado de semillas (semillas empapadas antes de la siembra), la adición de SA a una solución hidropónica o rociando plantas con solución SA, es favorable para el crecimiento de las plantas y ayuda a protegerlas estrés abiótico ( Hayat et al., 2010 ). Por ejemplo, la preparación de semillas con SA aumentó las actividades de las enzimas antioxidantes en guisantes jóvenes ( Pisum sativum L.) y conduce a la síntesis de novo de SA ( Szalai et al., 2011 ). Cuando la albahaca dulce ( Ocimum baslicumL.) se rociaron las plantas con cítrico y SA, suplementado con un agente tensioactivo, el patrón de adquisición de nutrientes de la raíz cambió para asimilar más boro y azufre, mejorando así su absorción al brote de la planta, aumentando así la biomasa fresca y la eficiencia fotosintética ( Ghazijahani et al. , 2014 ). Además, en las plantas de trigo ( Triticum aestivum ) el estrés abiótico causado por el insecticida clorpirifos fue mitigado mediante la pulverización de SA exógeno; probablemente debido a una mejora de la actividad de las enzimas antioxidantes. Además, SA pudo evitar la absorción de clorpirifos en plantas de trigo ( Wang y Zhang, 2017). Sin embargo, las aplicaciones exógenas de SA a menudo se llevan a cabo hasta la escorrentía, con la posibilidad de que ingresen a través de los estomas y que el daño mecánico suave pueda inducir los mecanismos de defensa ( Benikhlef et al., 2013 ). Sin embargo, no se han descrito los mecanismos implicados en la asimilación y / o transporte de SA en estas condiciones.
Se ha demostrado que la cutícula es apenas permeable al SA, a menos que se convierta en una forma volátil ( Figura 3 ). MeSA es un derivado volátil de SA y actúa como una señal de defensa aérea ( Tabla 1 ) ( Koo et al., 2007 ; Park et al., 2007 ). El MeSA se moviliza a través del floema para activar el SAR ( Yalpani et al., 1991 ; Kumar y Klessig, 2003 ). MeSA se activa cuando se invierte a SA por la actividad de esterasa de MeSA de la proteína de unión a SA 2 (SABP2) en el tejido sistémico ( Figura 2 ) ( Seskar et al., 1998 ; Park et al., 2007 , 2009 ; Vlot et al., 2007 , 2009 ; Vlot et al. al., 2008 ;Manosalva et al., 2010 ). De hecho, las mutaciones en SAMT o SABP2 comprometen el SAR ( Vlot et al., 2008 ). En conjunto, esta evidencia respalda el conocimiento de que el transporte de SA y MeSA sirve como una señal de floema móvil de larga distancia y que se debe llevar a cabo una homeostasis correcta para una activación exitosa de la SAR. Si bien SA pertenece a un mecanismo orquestado que induce SAR, no es el único, pero es un actor fundamental en la activación de una tarea tan significativa de las plantas frente al ataque de patógenos.
¿Qué esperar del transporte de Sudáfrica en el futuro?
Numerosos estudios confirman que SA juega un papel crucial durante el crecimiento y desarrollo de las plantas y, en particular, durante la inmunidad innata de las plantas ( Klessig et al., 2018 ). Por el contrario, el descubrimiento y la caracterización de los sistemas de transporte y las vías de señalización siguen siendo en gran medida esquivos. Si bien los enfoques genómicos, el análisis de seguimiento de SA radiomarcado y la inhibición de la compuerta del canal, han proporcionado información sobre la translocación SA intracelular y de larga distancia ( Dean y Mills, 2004 ; Park et al., 2007 ; Serrano et al., 2013 ; Zhu et al. , 2014 ; Vaca et al., 2017), hay demasiadas preguntas abiertas por responder sobre los mecanismos moleculares y celulares que guían el tráfico de SA intra y extracelular.
Ahora necesitamos ir más allá, hacia enfoques que permitan identificar nuevos portadores, receptores y objetivos de SA. Por ejemplo, el mapeo de interacciones proteína-proteína mediadas por SA puede ser una herramienta adecuada para este objetivo. Es probable que se encuentren más transportadores de tipo MATE y ABC involucrados en el transporte de SA, ya que se ha informado que estas familias de transportadores transportan tal diversidad de productos químicos, incluidas otras fitohormonas ( Zhang et al., 2014 ; Hwang et al., 2016 ). Los enfoques de interacción proteína-proteína de membrana y resonancia de plasmón de superficie de transmisión (TSPR), entre otros, podrían ofrecer una gran comprensión del nuevo transporte y receptores de SA ( Lertvachirapaiboon et al., 2018). Por ejemplo, en el futuro seremos capaces de monitorear la distribución de grupos de SA intracelulares mediante el desarrollo de imágenes de biosensores, utilizando estos receptores SA recientemente identificados ( Jones, 2016 ).
Además, se han utilizado modelos matemáticos para predecir el transporte de fitohormonas y las vías de señalización ( Voß et al., 2014 ), por ejemplo, el caso del transporte celular y de larga distancia de auxina en el tabaco y Arabidopsis thaliana , respectivamente ( Hošek et al., 2012 ; Boot et al., 2016 ). Además, para predecir la inducción secuencial de los portadores de flujo y de flujo de auxina en la regulación de la emergencia de la raíz lateral en Arabidopsis thaliana ( Péret et al., 2013 ). Las predicciones de modelado son útiles para seleccionar sistemas experimentales apropiados y generar modelos hipotéticos de transporte SA ( Otto et al., 2018), que en paralelo con las observaciones experimentales será una poderosa herramienta para desarrollar y establecer modelos del mecanismo de regulación del transporte SA.
Lea También: Las carnes más caras del mundo se venden en Venezuela







